Minden egyes ember csak szüleihez képest 60 új mutációt hordoz, amelyek a szülők ivarsejtjeiben, azok érése, kialakulása során jelentek meg. Hogy egy kicsit jobban számszerűsítsük, ez azt jelenti, hogy mindössze a jelenleg élő kb. 7 milliárd emberben, közvetlen elődeikhez képest, száz milliárd új mutáció jelent meg a fogantatás pillanatában, vagyis a kb. 3 milliárd bázispárnyi emberi genom minden egyes nukleotidja átlagban több tucatszor mutálódhatott csak ebben az evolúciós szempontból szűk időablakban. És mindez elenyésző ahhoz képest, ami testi sejtjeinkben történik, ahol az ivarvonalt érintő mutációk sokszorosa alakul ki az életünk során (egyes becslések szerint egy hatvan éves ember belében levő sejtek összességében minden egyes genomi pozícióban hordoznak valamilyen mutációt). A mutációk egy része egyszerűen a sejt DNS-másoló molekuláinak tévedésére vezethetők vissza, sokan azonban környezetei tényezők (UV-sugárzás, dohányfüst, stb.) számlájára írhatók.
Minden egyes ember csak szüleihez képest 60 új mutációt hordoz, amelyek a szülők ivarsejtjeiben, azok érése, kialakulása során jelentek meg. Hogy egy kicsit jobban számszerűsítsük, ez azt jelenti, hogy mindössze a jelenleg élő kb. 7 milliárd emberben, közvetlen elődeikhez képest, száz milliárd új mutáció jelent meg a fogantatás pillanatában, vagyis a kb. 3 milliárd bázispárnyi emberi genom minden egyes nukleotidja átlagban több tucatszor mutálódhatott csak ebben az evolúciós szempontból szűk időablakban. És mindez elenyésző ahhoz képest, ami testi sejtjeinkben történik, ahol az ivarvonalt érintő mutációk sokszorosa alakul ki az életünk során (egyes becslések szerint egy hatvan éves ember belében levő sejtek összességében minden egyes genomi pozícióban hordoznak valamilyen mutációt). A mutációk egy része egyszerűen a sejt DNS-másoló molekuláinak tévedésére vezethetők vissza, sokan azonban környezetei tényezők (UV-sugárzás, dohányfüst, stb.) számlájára írhatók.
Ennek az óriási mutáció-dömpingnek azonban csak töredéke hasznos a szervezet számára, a mutációk jelentős része nem oszt, nem szoroz (szakzsargonban neutrális), és a hasznosnál még mindig sokkal-sokkal több kifejezetten káros mutáció alakul ki, ami vagy működésképtelen és elpusztuló sejtet eredményez, vagy , ami még rosszabb, a nyakló nélküli proliferáció, vagyis a rák előszobáját jelentik.
Így aztán nem meglepő, hogy a legtöbb sejtben szofisztikált molekuláris mechanizmusok alakultak ki, hogy a mutációk mennyiségét a lehető minimumon tartsák. Különböző mutáció-fajták némileg különböző felismerő és javító-rendszereket igényelnek és a 2015-ös kémiai Nobel díjat ezeknek a molekuláris komplexeknek a feltárásáért ítélte oda a bizottság.
)
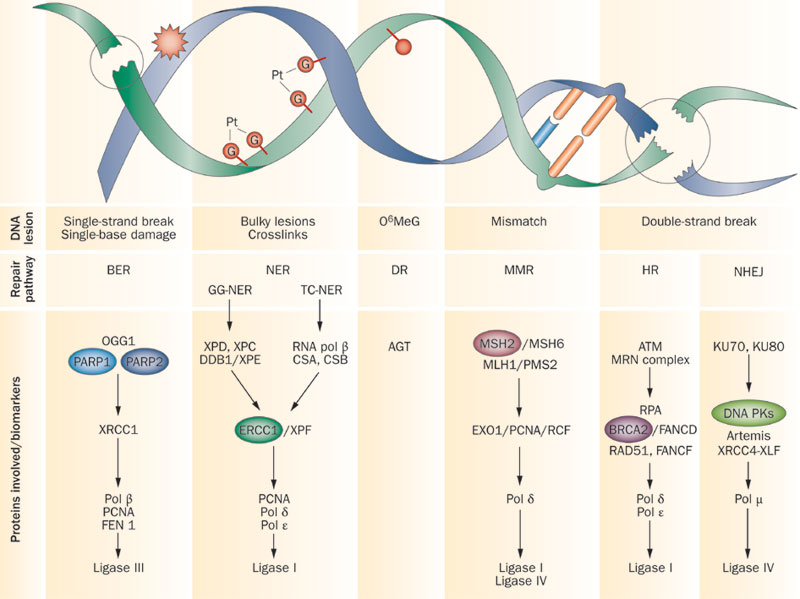
Konkrétabban az ismert hibajavítómechanizmusok közül három felfedezése ért most díjat:
- a NER (nem röhög!!), vagy teljes nevén nucleotide excision repair mechanizmus a különböző környezeti tényezők, pl. az UV-sugárzás hatására a DNS kettős spiráljában kialakuló keresztkötéseket és léziókat javítja ki, úgy, hogy a teljes, meghibásodott nukleotidát helyettesít, és a jelenleg a Yale-en dolgozó, török származású Aziz Sancar fedezte fel;
- a BER, azaz base excision repair, akkor kapcsol be, amikor a DNS egyes bázisai (vagyis az egyes nukletidok alegységei) hibásodnak meg. Ez egy meglehetősen gyakori folyamat, mert a DNS egy inherensen instabil molekula, aminek a komponensei könnyen lépnek olyan rekciókba, amelyek eredményeként megváltoznak. Például a citozin könnyedén alakul uracillá, amit az uracil-DNS glikoziláz nevű enzim ismer fel és javít ki, ezt fedezte fel Thomas Lindahl;
- végül a MMR, mismatch repair, a DNS másolás közben bekövetkező hibákat javítja ki. A DNS két szála komplementer, vagyis ahol az egyik szálon adenin (A) van, ott vele szemben, a másik szálon timin (T), illetve a citozinek (C) egy-egy guaninnal (G) képeznek párt. Mindez, mint arra a kettős spirál leírásakor már Francis Crick és James Watson is rámutatott, egy nagyon elegáns és kézenfekvő mechanizmust kínál a DNS másolására: a két szálat, ha kettéválasztjuk, akkor mindegyik természetes templátja lehet egy újonnan szintetizálódó szálnak. A műveletet DNS polimeráznak nevezett enzimek végzik, amelyek ugyan elég pontosak, de nem tökéletesek. Így időnként nem a komplementer nukleotidot építik be. Ezek a tévedések, mismatchek, akár veszélyes mutációk is lehetnek, nem véletlen, hogy a sejt tűzzel-vassal igyekszik őket írtani. Ennek a javító komplexnek a működését írta le a harmadik díjazott Paul Modrich.
Mivel meglehetősen biológiai jellegű felfedezésekért járt (ismét) a kémiai Nobel, ismét fellángolt persze a vita, hogy nem igazságtalan-e, hogy a leginkább Alfred Nobel munkásságához köthető díjat ismét nem vegyészek kapták. A valóságban persze nincs itt gond, hiszen a sejten belüli molekuláris folyamatok éppúgy kémiailag érdekesek, mintha csak egy kémcsőben vizsgálnánk dolgokat, és egy ilyen felfedezés fontosságát nem a reakció milliője határozza meg.
Chemistry is chemistry no matter where it happens - the cell is just a context for some fascinating and beautiful chemistry. #NobelPrize
— David K Smith (@professor_dave) October 7, 2015
Egyébként különös egybeesés, vagy sem, de az egyik legrangosabb élettudományi kitüntetést (amit sokan a Nobel előszobájaként emlegetnek), a Lasker-díjat idén épp olyan alapkutatásért ítélték oda, amelyik azt tisztázta, hogy a sejtek miként ismerik fel, ha sérült a DNS. A három Nobel-díjas kutatásával megegyező fontosságú dolog ez, s hogy a két díjazott csoport közt nem találunk átfedést, az jól mutatja, hogy ma már nagyon-nagyon nehéz meghatározni, hogy ki az a max. 3 személy (a Nobel díj esetében), akinek a munkája abszolút nélkülözhetetlen volt az adott felfedezéshez. A tudományos kutatás egy egyre inkább kollaboratív tevékenység, ennek megfelelően, érvelnek többen is, inkább nagyobb csoportokat, területeket kellene díjazni.
[Szerkesztői megjegyzés: a Meetup keretében nem is olyan régen volt már szó arról, miként vizsgálhatjuk a hibajavításhoz hasonló mechanizmusokat és remélhetőleg hamarosan még szolgálhatunk kapcsolódó előadásokkal. Watch this space! :-)]
(A poszt eredetileg a Science Meetup blogjában jelent meg.)