 A biológia 21. századi nagy ígéretei közül, az egyéni genomszekvenciák mellett még mindenképpen említést érdemel a szintetikus biológia. Durva leegyszerűsítésben ez mindazoknak a törekvéseknek a gyűjtőneve, amelyek célja tetszőleges (de többnyire kiemelkedő ipari jelentőségű) anyagok előállítása genetikailag módosított élőlények (az esetek többségében baktériumok) segítségével.
A biológia 21. századi nagy ígéretei közül, az egyéni genomszekvenciák mellett még mindenképpen említést érdemel a szintetikus biológia. Durva leegyszerűsítésben ez mindazoknak a törekvéseknek a gyűjtőneve, amelyek célja tetszőleges (de többnyire kiemelkedő ipari jelentőségű) anyagok előállítása genetikailag módosított élőlények (az esetek többségében baktériumok) segítségével.
Gondoljunk növényi anyagokból műanyagat előállítható bacikra, vagy fényérzékeny biofilmekre; a lehetőségek ha nem is végtelenek, de mindenképpen igen széles skálán mozognak. Látszólag, néhány fontos enzimet kódoló gén bejuttatásával, szinte kívánság szerinti kémiai láncreakció programozható – persze azért a valóság általában lényegesen bonyolultabb. Bonyolultabb, mert ezek a mikróbák a beléjük táplált útvonalakon kívül még egy sereg más reakciónak is otthont adnak, elsősorban olyanoknak amelyek a saját fennmaradásukhoz és szaporodásukhoz szükségesek, de nemcsak. És minden (a kívánt folyamat melleti) fölösleges folyamat csökkentheti a célreakció hatékonyságát, hiszen az organizmus energiáját és forrásait emésztik el. (Az már csak hab a tortán, hogy a saját maga által fölöslegesnek ítélt génektől az élőlények hajlamosak „megszabadulni“ (azok mutációkat szednek össze és működésképtelenekké válnak), így egy-egy ipari fermentorban könnyen elszaporodhatnak a potyázók, amennyiben nem biztosítjuk be genetikai trükkökkel, hogy ez ne következzen be.) Ezért aztán mindig nagy érdeklődés övezte azokat a baktériumokat, amelyek minimális számú génnel rendelkeznek: kevesebb saját gén, kevesebb lehetőség az energiák és tápanyagok „rossz“ felhasználására.
A technikai buktatók ellenére a szintetikus biológia igen ígéretes, nem véletlen, hogy Craig Venter is rástartolt a témára: mind a minimális genom, mind az iparban esetlegesen felhasználható, új enzimek kutatása terén igencsak aktív volt az utóbbi években. (A napokban derült ki, hogy már tavaly ősszel szabadalmi kérelmet nyújtott be, egy „szintetikus organizmus“ létrehozásásra.)
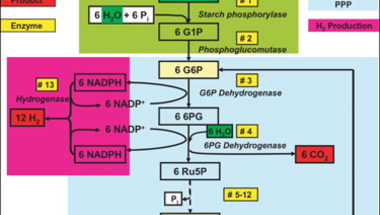
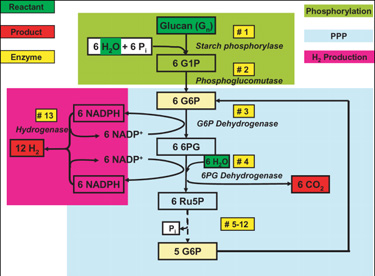
Persze egy minimális saját genom is igényel valamennyi energiát, így néhány purista arra törekszik, hogy pusztán csak enzimek összeöntésével érjék el a kívánt célt (persze azért az enzimek előállítása még nem megy in vitro, szóval ez azért nem teljesen „sejtmentes“ megoldás). Egy amerikai kutatócsoport most épp 13 különböző forrásból (növény, állat, élesztő és baktérium) származó enzim segítségével a növényi szövetekben előforduló keményítőből hidrogént állított elő. A reakció vízből és keményítőből indul ki, és az optimális 30°C-on hidrogén mellett szén-dioxidot termel (mivel ez friss növényi anyagból, azaz megújuló forrásból származik, netto nem jelent szennyezést). [C6H10O5 (l)+7 H2O (l)→12 H2 (g)+6 CO2 (g), ahol l = folyadék, g = gáz] A hidrogén üzemanyagcellákban energiaképzésre használható fel, így a folyamat ipari és környezetvédelmi szempontból egyaránt jelentős, s még az ára is viszonylag kedvező ($~2/kg H2) – ez a finomítások során még valszleg javulni is fog.
Igazából az egész dologgal egyetlen gond van: hogy a kiindulási anyag, a keményítő, nem a leggyakoribb növényi glükóz-polimer. Utóbbi titulus a nehezebben lebontható cellulóznak jut, s ha sikerülne elérni, hogy ez legyen a hidrogén előállítás kiinduló vegyülete, az akár egy kisebbfajta új ipari forradalom kezdetét is jelenthetné.
Zhang YP, Evans BR, Mielenz JR, Hopkins RC, Adams MW (2007) High-Yield Hydrogen Production from Starch and Water by a Synthetic Enzymatic Pathway. PLoS ONE 2(5): e456. doi:10.1371/journal.pone.0000456