Az új generációs szekvenáló készülékek megjelenésével a genom szekvenálás ára egészen elképesztő módon bedőlt. Így olyan kísérletek váltak lehetővé, amelyekről korábban csk álmodni lehett: míg az első emberi genom megszekvenálása milliárd dolláros fényűzés volt, ma már néhány ezer dollárból teljes genomokat határoznak meg.
Az egyik fontos csapásirány természetesen a különböző genetikai okokra visszavezethető betegségek kialakulása mögött rejlő DNS változások feltéképezése. És itt nemcsak a klasszikus mendeli betegségekre tessenek gondolni, hanem egy olyan "csendes" gyilkosra is mint a leukémia.
A leukémia a rák egyik formána, ahol a vérképző őssejtek (HSC) kattannak be és kezdenek korlátok nélkül osztódni. Az elváltozás hátterében olyan gének mutációi állnak, amelyek egyébként a pontos sejtosztódást szabályoznák. Ha ezek elromlanak a sejt előbb nyakló nélkül osztódni kezd, s mivel minden osztódás egyben DNS másolással is jár, ami szintén növeli az esélyét annak, hogy újabb hibák, mutációk csúsznak be, csak idő kérdése, hogy létrjöjjön a káros, terjeszkedésre (metasztázisra) képes, kvázi elpusztíthatatlan daganat.
A betegség tanulmányozására költött számolatlan pénznek annyi haszna volt, hogy már eddig is világos volt, több mutáció szükséges, ahhoz, hogy egy rákos transzformáció bekövetkezzen. De csak most jutott oda a technológia, hogy ezt szinte lépésről-lépésre követni tudjuk, egy beteg tumorát a betegség különböző fázisaiban vizsgálhatjuk bázispárnyi pontossággal.
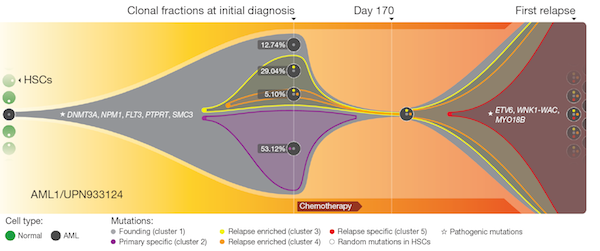 A mellékelt ábrán az látható, hogy miként változott egy leukémiás (AML) beteg rákos sejtpopulációjának összetétele a kór lefolyása alatt. Jól megfigyelhető, hogy a kezdeti daganatot egyetlen klón sejtjei alkotják: a szürke szín jelzi azokat a kezdeti mutációkat, amelyeket a kezelésre érkező beteg összes malignus sejtjében észleltek. Aztán fokozatosan újabb mutációk is kialakultak, amelyet a további színek jeleznek. Ezek közül egy (a lila) előnyt biztosított a daganaton eblül, így az ezt is hordozók többségbe kerültek. De aztán jött a kemoterápia, ami sikeresen kiírtotta ezeket a sejteket, és megcsappantotta a másik két (sárga és narancs) mutációt hordozó populációt is. De kiírtani utóbbit nem tudta, így csak idp kérdése volt, hogy ezek közt megjelenjenek a rezisztenicát biztosító mutációk (piros), amelyekkel már a terápiák nem tudtak mit kezdeni így a diagnózis után két évvel a beteg elhunyt.
A mellékelt ábrán az látható, hogy miként változott egy leukémiás (AML) beteg rákos sejtpopulációjának összetétele a kór lefolyása alatt. Jól megfigyelhető, hogy a kezdeti daganatot egyetlen klón sejtjei alkotják: a szürke szín jelzi azokat a kezdeti mutációkat, amelyeket a kezelésre érkező beteg összes malignus sejtjében észleltek. Aztán fokozatosan újabb mutációk is kialakultak, amelyet a további színek jeleznek. Ezek közül egy (a lila) előnyt biztosított a daganaton eblül, így az ezt is hordozók többségbe kerültek. De aztán jött a kemoterápia, ami sikeresen kiírtotta ezeket a sejteket, és megcsappantotta a másik két (sárga és narancs) mutációt hordozó populációt is. De kiírtani utóbbit nem tudta, így csak idp kérdése volt, hogy ezek közt megjelenjenek a rezisztenicát biztosító mutációk (piros), amelyekkel már a terápiák nem tudtak mit kezdeni így a diagnózis után két évvel a beteg elhunyt.
Természetes szelekció folyt itt, egy szervezeten, sőt ott is egy daganaton belül. A maga, mi szemszögünkből könyörtelen, de egyszerű logikája szerint tette a dolgát: mutációk jöttek létre, és amelyek jobb fennmaradást, hatékonyabb osztódást biztosítottak, azok rögzültek is. Végül persze a tumor a saját halálát is okozta, hiszen gazdája halálával neki is vége lesz, de ahogy kint, "nagyban", úgy itt bent kicsiben is igaz: a szelekció nem tervez, nem lát előre, csak az ott és akkor mérhető előnyöket favorizálja.
Ding L, Ley TJ, Larson DE, Miller CA, Koboldt DC, et al. (2012) Clonal evolution in relapsed acute myeloid leukaemia revealed by whole-genome sequencing Nature doi:10.1038/nature10738
 Sosem fogjuk megtudni, hogy min is törhette a fejét, a ma csak Ötzi néven ismert prehisztorikus alpesi juhász, amikor egy tavaszi napon egy nyílvessző fromájában utolérte a végzete. Abban viszont teljesen biztosak lehetünk, hogy sem akkor, sem addigi élete során még véletlenül sem gondolt arra, hogy azon első pár tucat (száz ?) ember között lesz, akinek teljes genetikai állományát felfejtik majd.
Sosem fogjuk megtudni, hogy min is törhette a fejét, a ma csak Ötzi néven ismert prehisztorikus alpesi juhász, amikor egy tavaszi napon egy nyílvessző fromájában utolérte a végzete. Abban viszont teljesen biztosak lehetünk, hogy sem akkor, sem addigi élete során még véletlenül sem gondolt arra, hogy azon első pár tucat (száz ?) ember között lesz, akinek teljes genetikai állományát felfejtik majd.


 Sporadikusan jelentkező "no comment" rovatunkban, most a
Sporadikusan jelentkező "no comment" rovatunkban, most a 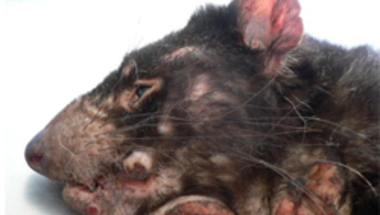
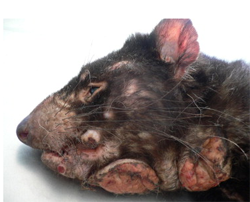 Van az úgy, hogy egy blognak is jól jönne egy szerkesztő, mert akkor két szerző nem dolgozik egyszerre ugyanazon a témán :-). De
Van az úgy, hogy egy blognak is jól jönne egy szerkesztő, mert akkor két szerző nem dolgozik egyszerre ugyanazon a témán :-). De



 Valami bűzlik, ha nem is Dániában, de azért hozzá elég közel: pusztán a
Valami bűzlik, ha nem is Dániában, de azért hozzá elég közel: pusztán a 
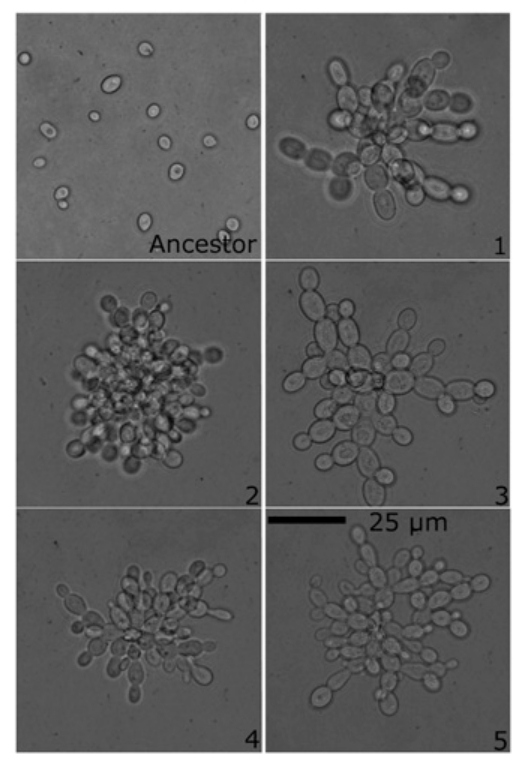 Modellszervezetként a Saccharomyces cerevisiae sörélesztőt használták, szelekciós nyomásként pedig a nehézkedést, mivel a több sejtből álló csomók hamarabb lesüllyednek a folyadék aljára, mint az egy sejtből állók, így egyszerűen elkülöníthetők az esetleg megjelenő többsejtű telepek. Rázatva növesztett élesztőkultúrákat állni hagytak háromnegyed órán át, majd a cső aljára ülepedett sejteket friss táptalajra helyezték. Majd az első hét után áttértek a 100 x g végzett tíz másodperces centrifugálásra, nyilván azért, mert így gyorsabb volt. Nem meglepő módon az evolúció itt is működött, hatvan átoltás után jelentősen csökkent az ülepedési idő, a kultúrákban nagy méretű, hópehelyszerű telepek jelentek meg, ezek láthatóak az első ábrán. Ami érdekes, hogy a kísérletet tízszer ismételték meg és mindannyiszor nagyon hasonló fenotípust mutattak a telepek, az egyes képek sarkában látható szám ugyanis a kísérlet sorszáma, vagyis az egyes pelyhek egymástól teljesen független evolúció termékei.
Modellszervezetként a Saccharomyces cerevisiae sörélesztőt használták, szelekciós nyomásként pedig a nehézkedést, mivel a több sejtből álló csomók hamarabb lesüllyednek a folyadék aljára, mint az egy sejtből állók, így egyszerűen elkülöníthetők az esetleg megjelenő többsejtű telepek. Rázatva növesztett élesztőkultúrákat állni hagytak háromnegyed órán át, majd a cső aljára ülepedett sejteket friss táptalajra helyezték. Majd az első hét után áttértek a 100 x g végzett tíz másodperces centrifugálásra, nyilván azért, mert így gyorsabb volt. Nem meglepő módon az evolúció itt is működött, hatvan átoltás után jelentősen csökkent az ülepedési idő, a kultúrákban nagy méretű, hópehelyszerű telepek jelentek meg, ezek láthatóak az első ábrán. Ami érdekes, hogy a kísérletet tízszer ismételték meg és mindannyiszor nagyon hasonló fenotípust mutattak a telepek, az egyes képek sarkában látható szám ugyanis a kísérlet sorszáma, vagyis az egyes pelyhek egymástól teljesen független evolúció termékei.
 Az talán már közhely-szintű, hogy az egyes emberi populációk földrajzi elterjedése és bőrszínük változatossága közt a szelekció teremt könnyen megfogható kapcsolatot: a világosabb bőrszín több D vitamin termelést biztosít, de kevésbé véd az UV-B sugárzástól, így csak ott alakulhatott ki, ahol a napsütés kevésbé volt intenzív. Az immunrendszerünk épp olyan jelleg, mint a bőrszín, így ugyanúgy az adott földrajzi környezet körülményei alakítják milyenségét.
Az talán már közhely-szintű, hogy az egyes emberi populációk földrajzi elterjedése és bőrszínük változatossága közt a szelekció teremt könnyen megfogható kapcsolatot: a világosabb bőrszín több D vitamin termelést biztosít, de kevésbé véd az UV-B sugárzástól, így csak ott alakulhatott ki, ahol a napsütés kevésbé volt intenzív. Az immunrendszerünk épp olyan jelleg, mint a bőrszín, így ugyanúgy az adott földrajzi környezet körülményei alakítják milyenségét.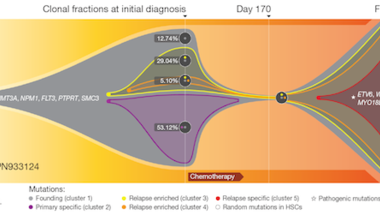
 A mellékelt ábrán az látható, hogy miként változott egy leukémiás (AML) beteg rákos sejtpopulációjának összetétele a kór lefolyása alatt. Jól megfigyelhető, hogy a kezdeti daganatot egyetlen klón sejtjei alkotják: a szürke szín jelzi azokat a kezdeti mutációkat, amelyeket a kezelésre érkező beteg összes malignus sejtjében észleltek. Aztán fokozatosan újabb mutációk is kialakultak, amelyet a további színek jeleznek. Ezek közül egy (a lila) előnyt biztosított a daganaton eblül, így az ezt is hordozók többségbe kerültek. De aztán jött a kemoterápia, ami sikeresen kiírtotta ezeket a sejteket, és megcsappantotta a másik két (sárga és narancs) mutációt hordozó populációt is. De kiírtani utóbbit nem tudta, így csak idp kérdése volt, hogy ezek közt megjelenjenek a rezisztenicát biztosító mutációk (piros), amelyekkel már a terápiák nem tudtak mit kezdeni így a diagnózis után két évvel a beteg elhunyt.
A mellékelt ábrán az látható, hogy miként változott egy leukémiás (AML) beteg rákos sejtpopulációjának összetétele a kór lefolyása alatt. Jól megfigyelhető, hogy a kezdeti daganatot egyetlen klón sejtjei alkotják: a szürke szín jelzi azokat a kezdeti mutációkat, amelyeket a kezelésre érkező beteg összes malignus sejtjében észleltek. Aztán fokozatosan újabb mutációk is kialakultak, amelyet a további színek jeleznek. Ezek közül egy (a lila) előnyt biztosított a daganaton eblül, így az ezt is hordozók többségbe kerültek. De aztán jött a kemoterápia, ami sikeresen kiírtotta ezeket a sejteket, és megcsappantotta a másik két (sárga és narancs) mutációt hordozó populációt is. De kiírtani utóbbit nem tudta, így csak idp kérdése volt, hogy ezek közt megjelenjenek a rezisztenicát biztosító mutációk (piros), amelyekkel már a terápiák nem tudtak mit kezdeni így a diagnózis után két évvel a beteg elhunyt.
 Hogy egy-egy oktopusz
Hogy egy-egy oktopusz 
 A biológia sajátos ága a biotechnológia, elvégre szép dolog a természet titkainak megfejtése, de még szebb, ha pénzt is sikerül csinálni belőlük. A
A biológia sajátos ága a biotechnológia, elvégre szép dolog a természet titkainak megfejtése, de még szebb, ha pénzt is sikerül csinálni belőlük. A